비행의 원리를 이해하기 위해 필요한 대기
대기는 지구를 지표면으로터 약 900 km를 둘러 싸고 있는 공기층의 공간을 의미한다. 공기는 주로 78% 질소, 21% 산소 등등으로 구성이 되어 있다.
지표면으로부터 11km 상공까지 수증기가 또한 다양하게 존재한다. 일정 공기에 실제 수증기의 양은 온도와 실제 공기가 대량의 물이 있는 지역을 최근에 통과했는지에 따라서 달라진다. 일반적으로 온도가 높을수록 특정 공기량에 포함된 수증기의 양은 증가한다.
공기는 무게가 있으며 또한 압축이 가능하다. 고도가 증가함에 따라 공기의 압력과 밀도 온도 모두 감소하게 된다.
항공기는 비행을 유지하기 위해 공기중을 움직이며 압력,밀도,온도에 따라 항공기의 에너지가 변화하며 영향을 받게 된다.
이제 그 영향들이 어떻게 서로 상호작용을 하는 지 알아보자.
알지만.. 잠시 살펴봐야할 법칙들
이상기체의 법칙 , Ideal Gas Law 또는 Universal Gas Law
이상기체의 방정식은 다음 법칙들의 합을 정리한 식이기도 한다.
이상기체의 방정식 = 보일의 법칙+샤를의 법칙+아보가드로의 법칙+게이뤼삭의 법칙
( 각 법칙에 대한 설명은 하단에 별도로 설명)
이상기체의 방정식
( {\displaystyle P}
: 압력, {\displaystyle V}
: 부피 , T : 절대온도,
: 기체 분자의 수 ,{\displaystyle R}
: 이상기체 상수)
여기서 밀도(ρ)는 특정 부피 당 기체분자의 수이므로 ρ = n/V 로 정의할 수 있고 압력, 밀도, 온도와의 상관관계는 다음과 같다.
P/ρT = constant
P : 압력, ρ: 밀도, T: 온도
그들의 관계 !!
[ 밀도에 대한 압력의 영항 ]
공기는 기체이며 쉽게 압축되거나 팽창 될수 있다. 공기가 압축되면 주어진 부피에서 분자 또는 질량의 수가 증가하고 밀도가 높아진다. 반대로, 공기가 팽창함에 따라, 원래의 체적은 더 적은 분자를 함유하고 밀도는 감소한다. 따라서 밀도는 압력에 비례한다.(즉, 압력이 두 배가되면 밀도도 두 배가 된다.). 단, 온도가 일정하다는 조건이다.
[ 밀도에 대한 온도의 영향 ]
공기가 가열됨에 따라, 분자는 가속화되는 경향이 있고 그 사이의 간격은 증가한다. 따라서, 주어진 부피는 더 적은 분자를 함유하고 공기 밀도는 감소한다. 반대로, 공기가 냉각되면 분자 운동의 정도가 감소하고 주어진 부피는 더 많은 수의 분자를 포함하므로 밀도가 증가한다. 공기 밀도는 온도에 반비례한다. (즉, 온도가 밀도를 두 배로하면). 단, 압력이 일정하다는 조건하이다.
[ 밀도에 대한 고도의 영향 ]
고도가 증가함에 따라 압력과 온도가 모두 감소한다. 온도의 강하는 밀도의 증가를 초래하고, 압력의 저하는 밀도의 감소를 초래한다. 이 요인들은 서로 대립적으로 작용하지만 압력은 밀도에 대해 지배적인 영향을 미친다.. 따라서 압력, 온도 및 밀도는 모두 고도가 높아짐에 따라 감소한다.
[ 밀도에 대한 습도의 영향 ]
먼저 , 공기가 완전히 건조하다고 가정한다. 실제로 대기 중에는 항상 특정 양의 수증기가 존재하는데, 이는 장소와 날마다 다르다.. 공기가 수증기를 함유하고있을 때 수증기가 건조한 공기보다 밀도가 낮기 때문에 공기의 밀도가 감소한다.. 표준 해수면 조건에서 수증기의 밀도는 0.760 kg/m3 인 반면, 건조한 공기의 밀도는 1.225 kg/m3입니다. 따라서 수증기는 건조한 공기만큼 5/8 정도 나간다. 이것은 주어진 부피에 대해 최대 수증기가 포함되어 있고 완전히 건조한 경우 밀도가 가장 높을 때 밀도가 가장 낮다는 것을 의미한다. 결국 습도는 항공기 성능에 영향을 미친다.
참고로 다음 법칙들을 간단히 소개합니다.
[ 보일의 법칙 ]
온도가 일정할때 기체의 부피는 압력에 반비례한다.
조건 : 분자의 수가 일정
방정식 :
또는
Image from “NASA” https://www.grc.nasa.gov/WWW/K-12/airplane/aboyle.html
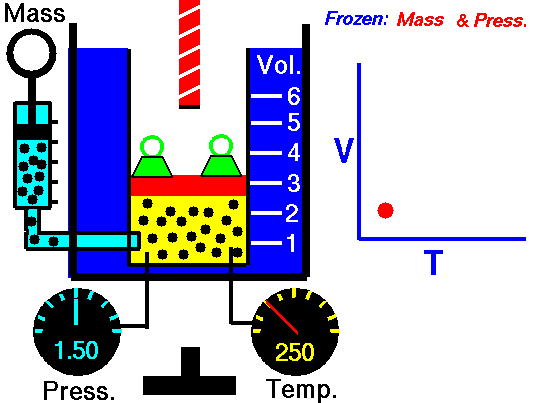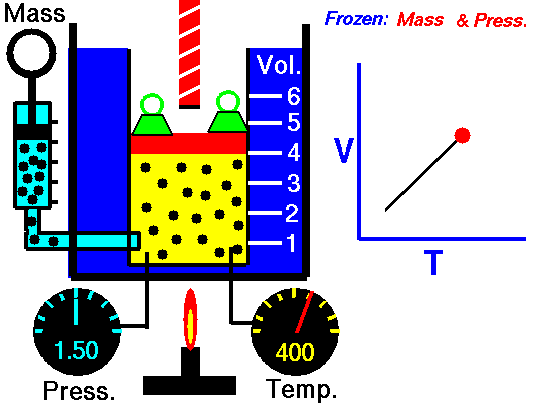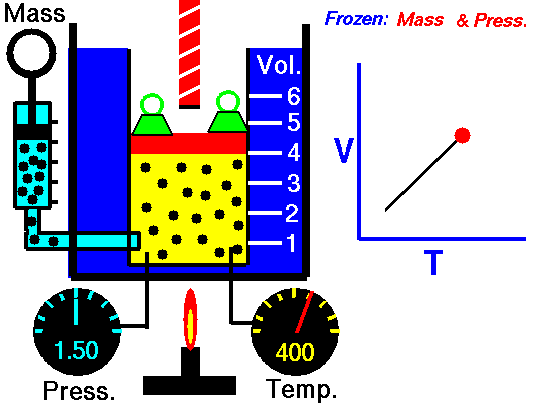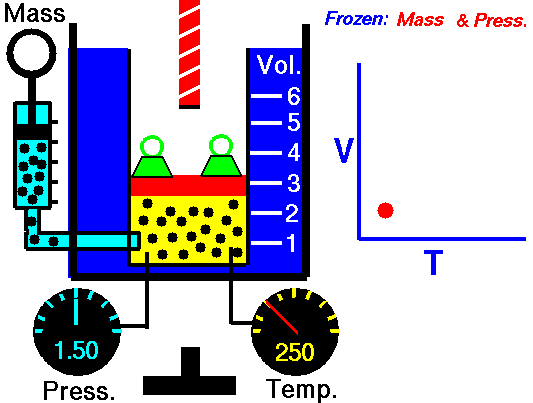
[ 샤를의 법칙 ]
압력이 일정할때 기체의 부피는 온도에 비례한다.
조건 : 분자의 수가 일정
방정식 :
또는
Image from “NASA ” https://www.grc.nasa.gov/WWW/K-12/airplane/aglussac.html
[ 아보가드로의 법칙 ]
기체의 종류에 상관없이 같은 온도, 같은 압력에서는 같은 부피를 가지며, 이때 분자의 수도 같음
방정식 :
또는
[ 게이뤼삭의 법칙 ]
압력은 온도에 비례한다.
방정식 :
또는